MurciaSalud
CSUR ERN
Introducción
Puede que esté leyendo este folleto porque un familiar ha sufrido una parada cardiaca. Esto no es sólo una tragedia para la familia, sino que además es una gran pérdida para la sociedad. Puede que se esté preguntando qué ocurrió y cómo pudo haberle ocurrido algo así a una persona joven y sana. O quizá su médico le ha sugerido que usted y su familia debieran someterse a alguna prueba por si lo que le ha ocurrido a su familiar pudiese heredarse.
En este folleto encontrará las posibles causas de parada cardiaca en jóvenes y en niños. En él encontrará información sobre:
- Qué ocurre después de que una persona sufra una parada cardiaca.
- Cómo funciona el corazón y por qué puede producirse una parada cardiaca.
- Por qué es importante que los familiares cercanos sean estudiados para averiguar si tienen la misma enfermedad ue el familiar fallecido y si es así, iniciar tratamiento médico.
- Las pruebas que su médico puede hacer para estudiarle a usted y a su familia.
- Consejos y hábitos de vida que debe seguir si tras estudiarle, se descubre que padece la enfermedad.
Intentaremos explicar todos los términos a lo largo del texto, pero si encuentra alguna palabra médica que no entiende, puede buscar su significado en el glosario de las últimas páginas.
Esperamos que con esta información tanto usted como su familia comprendan qué le ha pasado a su familiar y les sea de utilidad para comprender los pasos que se recomiendan seguir a partir de ahora.
Funcionamiento normal del corazón
El corazón es un músculo que se contrae continuamente y de forma regular para bombear sangre al resto del organismo. En su interior tiene una especie de circuito eléctrico que se activa cíclicamente y hace que el músculo cardiaco se contraiga. Si esta actividad eléctrica se altera puede afectar a la capacidad del corazón para bombear sangre adecuadamente.
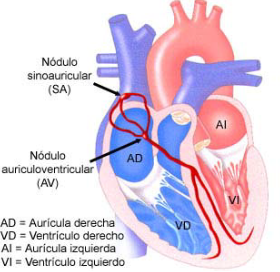
El corazón tiene cuatro cámaras (dos superiores que son las aurículas y dos inferiores que son los ventrículos). El estímulo normal que permite que el corazón se contraiga se origina en el nodo sinusal, que se encuentra en la aurícula derecha. Éste envía el impulso eléctrico al resto de la aurícula para que se contraiga y envíe la sangre a los ventrículos. El impulso eléctrico pasa de la aurícula a través de una estructura especial, que es el nodo auriculo-ventricular.
Cuando el impulso llega a los ventrículos, éstos se contraen y bombean sangre al resto del organismo. Cuando es necesario, el organismo produce ciertas sustancias que se vierten en la sangre para hacer que el corazón pueda contraerse con mayor rapidez. La actividad eléctrica del corazón puede detectarse mediante un electrocardiograma (ECG).
Concepto de parada cardiaca con y sin cardiopatía estructural
¿Qué es una parada cardiaca? ¿Qué es una parada cardiaca recuperada? ¿Qué es una muerte súbita?
Decimos que una parada cardiaca es una pérdida brusca del pulso y el conocimiento causada por un fallo inesperado de la capacidad del corazón para bombear eficazmente sangre al cerebro y a todo el organismo. Si el corazón deja de funcionar (parada cardiaca), el flujo sanguíneo se detiene, los órganos empiezan a fallar y en cuestión de minutos la persona muere (muerte súbita). Si el paro cardiaco puede detectarse y tratarse de inmediato, pueden evitarse daños serios a los órganos, daño cerebral o incluso la muerte (parada cardiaca recuperada o resucitada). La parada cardiaca ocurre de forma súbita cuando se produce de manera inesperada, brusca y espontánea. Algunas veces se producirá sin testigos, y puede hacerlo tanto durante el sueño como el ejercicio físico. La mayor parte de las paradas cardiacas se producen por una causa cardiaca. El mecanismo por el que se produce la muerte es una alteración del ritmo cardiaco en los ventrículos (arritmia ventricular). Esta arritmia puede hacer que los ventrículos latan demasiado rápido, demasiado lento o incluso que el corazón pueda pararse. Esta situación puede alterar la capacidad del corazón para bombear sangre y producir una caída muy importante de la tensión arterial. Si esta situación no se resuelve de forma precoz, el cerebro, el corazón y finalmente el resto de los órganos resultarán dañados seriamente y se producirá la muerte.
¿Cúal es la diferencia entre la parada cardiaca con cardiopatía estructural y la parada cardiaca sin cardiopatía estructural?
La parada cardiaca de origen cardiaco es una muerte repentina que se produce por una enfermedad cardiaca. En 1 de cada 20 casos de muerte de origen cardiaco no se encuentra una causa aparente incluso después de realizar una autopsia. Cuando nos encontramos en esta situación, decimos que nos encontramos ante una muerte súbita sin cardiopatía estructural.
Este texto está dedicado a las enfermedades que pueden producir una parada cardiaca en las que no se encuentra ninguna alteración estructural del corazón. Es decir, en las que el tamaño del corazón, sus cavidades, las válvulas y las arterias coronarias son normales. Estas enfermedades no son las que más frecuentemente producen muerte súbita y en ocasiones son difíciles de diagnosticar. Para ello se necesitan realizar una serie de pruebas cardiológicas y test genéticos.
Causas de parada cardiaca en nuestro medio
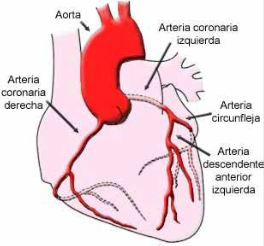
La primera causa de parada cardiaca en mayores de 40 años es la enfermedad coronaria. Como consecuencia del efecto nocivo de distintos agentes y factores de riesgo cardiovascular (hipertensión arterial, tabaco, diabetes, niveles elevados de colesterol en sangre) sobre las arterias coronarias, puede producirse una lesión y un coágulo de sangre que bloquea la arteria. Si esto ocurre, una parte del músculo cardiaco no recibe el aporte de sangre necesario para obtener oxígeno y se produce un infarto. En ciertas personas, cuando se produce el infarto puede originarse además una arritmia maligna que puede producir la muerte. En las ilustraciones que se muestran a continuación pueden observarse la distribución de las arterias coronarias y las válvulas cardiacas respectivamente.
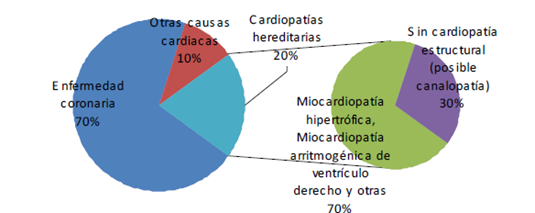
En nuestro país, aproximadamente el 70% de las muertes súbitas en menores de 60 años se producen por enfermedad coronaria. El 20% se debe a cardiopatías hereditarias y el 10% restante se debe a diferentes causas.

Las causas más importantes dentro del grupo de las cardiopatías hereditarias son la miocardiopatía hipertrófica y la miocardiopatía arritmogénica de ventrículo derecho, que suman entre las dos el 70% del total. El 30% restante se debe a un grupo de enfermedades conocidas como canalopatías, que pueden tener una causa genética y ser hereditarias.
Causas de parada cardiaca en nuestro país
Se calcula que cada mes se produce al menos 1 caso de muerte súbita por cada millón de habitantes, en una persona joven y aparentemente sana. Estos casos de muerte súbita son producidos por una enfermedad cardiaca genética con mucha probabilidad.
Enfermedades cardiacas que pueden producir parada cardiaca distintas de la enfermedad coronaria
Estas enfermedades son diagnosticadas sobre todo en menores de 35 años y algunas de ellas son hereditarias. Dentro de este grupo algunas enfermedades son detectadas fácilmente en personas sanas pero otras pueden no detectarse hasta que se produce el fallecimiento.
1.Miocardiopatías
Son anomalías del músculo cardiaco y generalmente son hereditarias:
- Miocardiopatía hipertrófica:En esta enfermedad las paredes del corazón son anormalmente gruesas sin que exista una causa que lo justifique. Para más información acerca de esta enfermedad puede dirigirse a la web: www.murciasalud.es/patologias
- Miocardiopatía arritmogénica del ventrículo derecho: Su característica principal es que las paredes del corazón presentan gran cantidad de grasa y tejido fibroso. Afecta preferentemente al ventrículo derecho. Para más información acerca de esta enfermedad puede dirigirse a la web: www.murciasalud.es/patologias
- Miocardiopatía dilatada: En ella todas las cámaras del corazón (aurículas y ventrículos) se encuentran agrandadas y bombean sangre con mayor dificultad. Si no se bombea suficiente cantidad de sangre se produce insuficiencia cardiaca. Para más información acerca de esta enfermedad puede dirigirse a la web: www.murciasalud.es/patologias
2.Enfermedades cardiacas congénitas
- En este grupo se incluyen anomalías de la estructura del corazón, que pueden estar presentes desde el nacimiento. Algunas de estas enfermedades pueden ser hereditarias aunque en la mayoría de los casos no lo son. En este grupo se incluyen:
- Enfermedades valvulares y enfermedades complejas, como la Tetralogía de Fallot.
- Anomalías en el recorrido de las arterias coronarias, que son las arterias que suministran la sangre para nutrir al músculo cardiaco.
3.Miocarditis
Es una inflamación del músculo cardiaco. Generalmente es debida a una infección vírica, aunque también puede ser una complicación de otras enfermedades o secundaria a ciertos medicamentos. No es hereditaria.
4.Enfermedades del tejido conectivo
Son enfermedades del tejido que fortalece y da elasticidad a los vasos sanguíneos y al músculo cardiaco. Como ejemplo podemos mencionar el Síndrome de Marfan y el de Ehler-Danlos. En estas enfermedades se pueden romper vasos sanguíneos importantes, como la arteria aorta (que transporta la sangre desde el ventrículo izquierdo del corazón al resto del organismo).
5.Anomalías de la conducción eléctrica
Son anomalías en el modo en el que el impulso eléctrico es conducido desde las aurículas a los ventrículos. Puede existir un bloqueo en el impulso eléctrico o existir una doble vía que puede originar un ¿cortocircuito¿ como en el Síndrome de Wolf-Parkinson-White.
6.Causas relacionadas con la toma de medicación y otras sustancias
Ciertos fármacos, así como drogas ilegales pueden producir como efecto secundario ciertas arritmias y a veces, muerte súbita.
7.Otras causas de parada cardiaca de origen no cardiaco
Otras enfermedades como la epilepsia o crisis severas de asma pueden ser causa, aunque infrecuente, de parada cardiaca. El tromboembolismo pulmonar (un trombo que se aloja en el interior de las arterias pulmonares) puede estar producido por muchas causas (enfermedades de la sangre, algunos tumores, inmovilización prolongada¿) y ser causa de síncope y muerte súbita.
Parada cardiaca sin cardiopatia estructural
Recordemos que en aproximadamente 1 de cada 20 casos de parada cardiaca no se encuentra una causa a pesar de realizar un estudio completo. Esta situación se conoce como parada cardiaca sin cardiopatía estructural. En el siguiente apartado describiremos las causas responsables de este síndrome.
¿Qué causa la parada cardiaca con necropsia normal?
Las causas responsables de este síndrome producen arritmias malignas y una parada cardiaca incluso cuando la persona no padece alteraciones en la estructura del corazón.
Existe un grupo de enfermedades conocidas como canalopatías, que afectan al funcionamiento eléctrico del corazón sin afectar a su estructura. Esto significa que sólo pueden ser detectadas en sujetos vivos y no en la autopsia. Existen diferentes tipos de canaloptías que incluyen:
- Síndrome de QT largo.
- Síndrome de Brugada.
- Defectos progresivos en el sistema de conducción.
- Taquicardia ventricular catecolaminérgica polimórfica.
- Fibrilación ventricular idiopática.
- Síndrome de QT corto.
CANALOPATÍAS
Son alteraciones causadas por anomalías en el ADN, conocidas como mutaciones. Normalmente son heredadas de los padres aunque, pueden ocurrir por primera vez en un paciente. Estas mutaciones afectan a ciertos genes que son responsables de la producción de los canales iónicos. Un ion es una sustancia química (como el sodio, el potasio o el calcio) que tiene una carga eléctrica e interviene en la transmisión del impulso eléctrico a través del músculo cardiaco. Los canales iónicos regulan el flujo eléctrico. Si estos canales no se comportan normalmente, el funcionamiento eléctrico del corazón se altera. La persona que padece una canalopatía se encuentra predispuesta a sufrir arritmias que en algunas ocasiones pueden producir una parada cardiaca.
A continuación vamos a describir los diferentes tipos de canalopatías, las pruebas necesarias para diagnosticarlas y el tratamiento que precisa cada una de ellas.
SÍNDROME DE GT LARGO
Es el tipo de canalopatía más frecuente y mejor conocida. Se presenta en 1 de cada 5000 individuos. En 6 de cada 10 individuos con síndrome de QT largo se consigue identificar los canales iónicos responsables. En la mayoría de las ocasiones son dos de los canales de potasio los responsables (regulan el movimiento de potasio desde el interior al exterior de la célula). En una pequeña proporción de individuos con este síndrome, el canal afectado es el canal del sodio (regula el paso de sodio desde el exterior al interior de la célula).
Como resultado de la alteración de estos canales se produce una alteración en la actividad eléctrica del corazón que se conoce como repolarización prolongada y esto produce que el corazón tarde más tiempo de lo normal en recuperarse eléctricamente después de cada latido. Esto puede observarse en el ECG mediante la prolongación del intervalo QT. Esta es la causa de que este síndrome se conozca como síndrome de QT largo.
¿Cuáles son los síntomas?
Los síntomas y la severidad varían según el tipo de canal implicado. También dependen de otras circunstancias como la edad, el sexo o la longitud del intervalo QT. Los varones tienen mayor probabilidad de sufrir síntomas antes de la pubertad, mientras que las mujeres suelen tener síntomas en la adolescencia o en la edad adulta temprana. Los familiares que han heredado la misma mutación pueden encontrarse en uno de los siguientes grupos: tienen un QT normal y no tienen síntomas; tienen un QT anormal y no tienen síntomas; tienen un QT anormal y tienen síntomas. El síntoma más común es la pérdida de conocimiento o síncope. Algunas veces las palpitaciones pueden ser otro síntoma molesto.
Las mutaciones del canal del potasio se asocian a parada cardiaca relacionada con el ejercicio y a algunos estímulos como un estrés emocional intenso. Las mutaciones del canal del sodio se asocian con parada cardiaca durante el sueño.
¿Cómo se diagnostica?
Primero necesitamos tener un ECG. Desafortunadamente, muchas personas que son portadoras del gen alterado tienen un ECG normal. Realizar ECG en repetidas ocasiones, pruebas de esfuerzo, o un registro de ECG durante 24h (Holter) puede ser útil, pero incluso tras realizar estas pruebas, el diagnóstico de la enfermedad puede ser difícil.
Tratamiento y recomendaciones.
Se debe evitar realizar ejercicio físico intenso y extenuante. Además hay que suprimir ciertos medicamentos que pueden empeorar esta enfermedad y aumentar el riesgo de complicaciones.
La necesidad de tratamiento se establece según el riesgo de sufrir una muerte súbita. Estadísticamente sabemos que las personas con mayor riesgo son aquellas que:
- Han sufrido una parada cardiaca resucitada.
- Sufren síncopes (pérdidas de conocimiento).
- Tienen un intervalo QT muy largo en el ECG.
- Tienen mutaciones en el canal del sodio.
- Mujeres jóvenes.
Los medicamentos más utilizados para tratar este síndrome son los betabloqueantes. Esta medicación bloquea el efecto de la adrenalina sobre el corazón y por tanto, bloquea los efectos que el ejercicio produce sobre el corazón. Son efectivos en las formas más frecuentes de síndrome de QT largo, porque reducen los síntomas y el riesgo de parada. Sin embargo, son menos efectivos en pacientes con mutaciones en el canal del sodio.
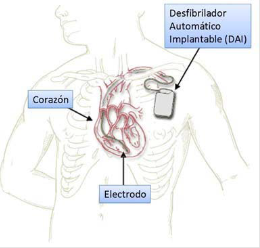
Marcapasos y DAI
Si una persona tiene un riesgo alto de sufrir una muerte súbita (por ejemplo, si ya ha sufrido una parada cardiaca o si los fármacos no controlan los síntomas adecuadamente) el médico puede recomendar el implante de un desfibrilador (DAI). Es una especie de marcapasos complejo que se coloca debajo de la piel y se une al corazón mediante unos cables. Este aparato puede detectar arritmias peligrosas para la vida y enviar una descarga eléctrica para restaurar el ritmo cardiaco normal.
Cirugía
Otra opción de tratamiento es cortar los nervios que liberan adrenalina y otras sustancias en el corazón. Esta operación se conoce como ¿Simpatectomía cervical¿ y se realiza en el lado izquierdo del cuello. Esta intervención se realiza en muy pocos casos.
SÍNDROME DE BRUGADA
Este síndrome fue descubierto a principios de los años noventa por unos cardiólogos catalanes (los hermanos Brugada). Es una enfermedad rara en los países occidentales pero es mucho más común en el sureste asiático, sobre todo entre hombres jóvenes de entre 30-40 años.
Se han encontrado mutaciones genéticas en el canal del sodio (el mismo que se encuentra afectado en el Síndrome de QT largo tipo III). Pero esta mutación sólo se detecta en un 20% de los pacientes que padecen el Síndrome de Brugada. Como resultado de esta alteración, se producen cambios en el ECG aunque el corazón es estructuralmente normal.
¿Cuáles son los síntomas?
Algunas personas con este síndrome pueden no tener síntomas en absoluto. Entre los que tienen síntomas, el más frecuente es el síncope. Algunas personas pueden notar palpitaciones. Y en algunos casos puede producirse una parada cardiaca que, en muchas ocasiones se produce mientras la persona duerme.
¿Cómo se diagnostica?
Primero necesitamos tener un ECG. Las alteraciones típicas de este síndrome pueden aparecer de forma mantenida o intermitentemente. Cuando un paciente de Síndrome de Brugada presenta fiebre, los cambios en el ECG pueden ser más evidentes y algunos pacientes pueden tener más riesgo de presentar arritmias durante estos episodios febriles.
Si los pacientes no presentan alteraciones en el ECG podemos realizar pruebas para realizar el diagnóstico. Son los llamados test de provocación. Para realizarlos se inyecta un medicamento antiarrítmico mientras se realiza un ECG. Los medicamentos que se utilizan más frecuentemente son la flecainida y la ajmalina.
El análisis genético no es muy útil para el diagnóstico del síndrome de Brugada porque las mutaciones se encuentran en una pequeña proporción de personas que padecen el síndrome.
Tratamiento y recomendaciones
En personas que han sufrido síncopes o arritmias malignas, el implante de un DAI es el tratamiento más efectivo. A pesar de que algunos medicamentos (como la quinidina) se utilizan en algunos casos, el tratamiento con medicación no es tan eficaz como el DAI.
Los pacientes que nunca han presentado una pérdida de conocimiento, que no tienen antecedentes familiares de muerte súbita, con ECG normal o prácticamente normal en los que la alteración aparece únicamente durante la prueba de provocación con fármacos tienen un riesgo muy bajo de presentar complicaciones. Aunque en estos pacientes no es preciso tomar ningún tratamiento, se aconseja acudir a revisiones periódicas en la consulta.
En ciertas ocasiones, la realización de un estudio electrofisiológico puede ser de utilidad para identificar aquellos pacientes que pueden necesitar un DAI. Por ejemplo, en pacientes que tienen un ECG con las alteraciones características de esta enfermedad de forma constante o en aquellos que han sufrido síncopes. Esta prueba consiste en llegar mediante unos cables que se introducen por las venas de la ingle hasta el corazón, realizar una serie de estímulos y comprobar si se producen arritmias peligrosas. En caso de que la prueba sea positiva, se aconsejará el implante de un DAI. Esta prueba se realiza con anestesia local y es excepcional que se produzcan complicaciones importantes. Para más información sobre el Síndrome de Brugada puede dirigirse a la web: Patologías
Otras causas cardiológicas menos frecuentes de parada cardiaca
Taquicardia ventricular catecolaminégica polimórfica
Es una enfermedad muy rara que podemos encontrarla en niños y gente joven, que produce un tipo de arritmia conocida como taquicardia ventricular polimórfica. Se asocia a la alteración de dos genes que fabrican dos proteínas que se encuentran dentro de las células: el receptor de la rianodina y la calsecuestrina. Estas proteínas regulan la liberación de calcio en el interior de la célula cardiaca. Si estas proteínas no funcionan adecuadamente se produce un aumento del calcio dentro de la célula y se favorece la aparición de arritmias.
¿Cuáles son los síntomas?
Algunas personas pueden no tener síntomas. Otras pueden presentar síncopes. La parada cardiaca puede producirse mientras se realiza ejercicio físico intenso o se sufre un estrés emocional muy importante. Esta enfermedad afecta fundamentalmente a niños, especialmente a varones.
¿Cómo se diagnostica?
El diagnóstico se realiza al registrar este tipo de arritmia mientras la persona realiza ejercicio físico. El análisis genético es útil para detectar a miembros de la familia que puedan estar afectados. La mutación del gen del receptor de la rianodina puede detectarse en un 70% de los afectados, mientras que la mutación del gen de la calsecuestrina sólo se encuentra en un 7% de los pacientes.
Tratamiento y recomendaciones
El tratamiento indicado son los betabloqueantes, que son muy eficaces. Además, se debe restringir la realización de ejercicio físico. Algunas personas con esta enfermedad podrían necesitar el implante de un desfibrilador (DAI).
Afectación progresiva del sistema de conducción cardiaco o síndrome de Lev-Lenegre
Es una enfermedad rara, en la cual, los impulsos eléctricos del corazón se conducen muy lentamente. Con el tiempo pueden producirse distintos tipos de ¿bloqueos¿. Cuando existe un bloqueo, el impulso eléctrico del corazón tiene dificultad o en ocasiones es incapaz de pasar desde las aurículas a los ventrículos, por lo que el ritmo cardiaco puede ser muy lento. Esta enfermedad también tiene una causa genética (mutación en el gen del canal del sodio), aunque no siempre se consigue identificar.
¿Cuáles son los síntomas?
Los síntomas más frecuentes son mareos y síncope. En ocasiones puede producirse una parada cardiaca.
¿Cómo se diagnostica esta enfermedad?
Mediante un ECG o un Holter. En ocasiones puede ser necesario realizar un estudio electrofisiológico. Si la persona afectada presenta una mutación en el canal del sodio, podremos encontrar esta mutación en algunos familiares.
Tratamiento y recomendaciones
Esta enfermedad requiere el implante de un marcapasos para prevenir la aparición de bradiarritmias (arritmias en las que el ritmo cardiaco es muy lento).
Fibrilación ventricular idiopática
La fibrilación ventricular es un tipo de arritmia que amenaza la vida. Los pacientes que sufren esta enfermedad no presentan signos de enfermedad cardiaca. Todas las pruebas cardiológicas son normales. Algunos pacientes presentan una mutación en el canal del sodio. El tratamiento consiste en implantar un DAI. Afortunadamente, es una enfermedad extremadamente rara.
¿Qué ocurre si es usted un familiar cercano de una persona que ha presentado una parada cardiaca?
¿Qué estudios familiares hay que realizar?
A continuación vamos a contestar a una serie de preguntas que probablemente se esté haciendo tanto usted como el resto de su familia.
¿Es necesario realizar pruebas a los familiares?
Si. Es importante realizar pruebas para averiguar si ha heredado la enfermedad.
¿Puede ocurrir que tras estudiar a una familia no se encuentren signos de la enfermedad?
Si. Esto ocurre en más la mitad de las familias. Las causas que pueden explicarlo son dos:
- La persona que ha sufrido una parada cardiaca no ha heredado la enfermedad de sus padres, sino que ha sido el primero de la familia en sufrir la mutación (por lo tanto sus hijos son las únicas personas que pueden heredar la mutación) o bien, el enfermo tiene otra causa de parada cardiaca no identificada que no es hereditaria.
- Algunos familiares pueden ser portadores de la enfermedad pero no mostrar signos de ella. Es difícil asegurar al 100% que un familiar no es portador de la mutación, excepto en aquellos casos en los que la mutación ha sido identificada en la persona que ha presentado la parada y se realiza un análisis genético para comprobar si el familiar porta esa misma mutación. Sin embargo, las personas que no muestran signos ni síntomas de la enfermedad presentan un riesgo muy bajo. Las personas con mayor riesgo son aquellas que presentan síntomas, han sufrido una parada cardiaca o presentan anomalías en el ECG y otras pruebas.
¿Qué ocurre si se encuentra una de estas enfermedades en su familia?
Si usted es diagnosticado de alguna de las enfermedades que hemos descrito anteriormente, necesitará un seguimiento médico independientemente de que reciba tratamiento o no.
Si es una persona joven, se le ha estudiado y su médico piensa que no está afectado, debería ser sometido a otra revisión pasado un tiempo. Esto es debido a que las alteraciones en el ECG pueden ser más evidentes dentro de unos años o a que las alteraciones pueden aparecen en unos ECG y en otros no.
Si en una persona que ha sufrido una parada cardiaca se identifica una mutación responsable de la enfermedad y un familiar no porta esa mutación, entonces se puede asegurar que esa persona no se encuentra afectada.
¿Qué tipo de estudio se realiza a los familiares?
Dado que las algunas enfermedades que producen parada cardiaca pueden heredarse, es importante estudiar a los familiares. A continuación vamos a describir qué pasos son necesarios para realizar este estudio.
Historia clínica
Es importante reunir todos los datos clínicos del fallecido, así como la información adicional descubierta por el forense y la policía. Por ejemplo, si una persona fallece durante el sueño nocturno podemos pensar en un Síndrome de Brugada. Por el contrario, si el fallecimiento se produce durante el ejercicio o un estrés emocional, pensaríamos en un Síndrome de QT largo o una Taquicardia ventricular catecolaminérgica polimórfica. Es también de vital importancia conocer cualquier medicación que la persona haya podido tomar antes de producirse la muerte. Y si es posible, es importante además recoger información de ingresos previos si los hubiese, así como ECG de reconocimientos médicos previos o de preoperatorios.
Su médico puede preguntarle si alguna vez ha notado síntomas como palpitaciones o si ha sufrido un síncope, lo que puede hacer sospechar una enfermedad cardiaca.
Exploración física
Una exploración física detallada puede ayudar a identificar si existe una enfermedad estructural cardiaca. Algunas enfermedades que afectan a la estructura del corazón pueden producir soplos y otros signos.
Electrocardiograma (ECG)
Con el ECG observamos la actividad eléctrica del corazón. Para ello se colocan electrodos en tobillos, muñecas y en el pecho. La siguiente imagen muestra un ECG normal.
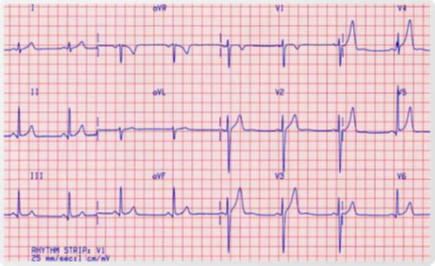
ECG de señal promediada o "potenciales tardíos"
Es un ECG más largo con el que podemos detectar alteraciones muy sutiles, por ejemplo, si el impulso eléctrico es conducido más lentamente de lo normal. Es muy útil en el estudio de la miocardiopatía arritmogénica de ventrículo derecho. Esta prueba requiere unos 5 minutos en realizarse.
Ecocardiograma
Utiliza ondas de ultrasonidos para observar la estructura del corazón. Es útil para el estudio de aquellas personas cuyo ECG muestra alteraciones que pueden ser producidas por muchos tipos de enfermedades cardiacas. Entre ellas ciertas enfermedades hereditarias como los distintos tipos de miocardiopatías.
Prueba de esfuerzo o ergometría
Esta prueba consiste en realizar un ECG mientras se realiza ejercicio en una cinta o en bicicleta. Con ello podemos detectar cambios en la actividad eléctrica que ocurre en el ejercicio. Esta prueba es particularmente importante en enfermedades como la miocardiopatía hipertrófica, miocardiopatía arritmogénica de ventrículo derecho, síndrome de QT largo o la taquicardia ventricular catecolaminérgica.
Holter
Es una especie de grabadora que se transporta en un cinturón. De él salen 4 ó 6 electrodos que se unen al pecho mediante unas pegatinas. Este aparato registra la actividad eléctrica del corazón desde 1 ó 2 días hasta 1 semana. Con esto podemos analizar la actividad eléctrica del corazón y detectar posibles arritmias.
Existen otras variantes de este tipo de dispositivo: el registrador de eventos y el ¿Reveal¿. El registrador de eventos es un aparato que puede activarse para grabar la actividad eléctrica del corazón cuando el paciente se nota síntomas (por ejemplo, palpitaciones o mareo).
El "Reveal" es un aparato que implantamos cuando es difícil grabar la actividad eléctrica del corazón cuando se producen síntomas porque estos se producen infrecuentemente. Por ejemplo, un síncope cada muchos meses. Este aparato es del tamaño de una batería de teléfono móvil y se implanta mediante una pequeña incisión (unos 2 cm) debajo de la piel en la zona submamaria. Este aparato detecta el ritmo cardiaco y puede grabar ciertas anomalías que puedan producirse. Cuando se producen los síntomas, el paciente debe presionar el botón de un pequeño mando y entonces el aparato grabará en su memoria la actividad eléctrica del corazón de los 20 minutos previos. El ¿Reveal¿ puede ser interrogado por un ordenador en el hospital y el médico puede ver la grabación. La batería del aparato puede durar hasta dos años.
Test de provocación farmacológica (ajmalina, flecainida adenosina y adrenalina)
Si se sospecha que puede padecer un síndrome de Brugada este test es de gran utilidad. Consiste en realizar un ECG mientras se inyecta medicación antiarrítmica (ajmalina o flecainida). Con esto podemos ver cambios en el ECG que son típicos de esta canalopatía.
La medicación se inyecta con un suero durante un período de tiempo corto (5-10 minutos) y después hay que permanecer monitorizado durante 20 minutos más. En raras ocasiones, 1 de cada 200 pacientes con Síndrome de Brugada pueden producirse arritmias al inyectar la medicación, por tanto, este test se realiza en un lugar adecuado, con los instrumentos y personal necesario para tratar cualquier complicación.
El test de adrenalina es útil para casos dudosos de síndrome de QT largo, puesto que tras inyectar este medicamento podemos ver una prolongación del intervalo QT que puede ayudarnos en el diagnóstico.
El test de adenosina puede realizarse durante el estudio del Síndrome de Wolf-Parkinson-White.
Cardiorresonancia magnética
Es una prueba inocua que no utiliza radiación. Se necesita inyectar una contraste a través de una vena del brazo. Mediante la resonancia podemos estudiar el corazón y especialmente, las características del músculo cardiaco. Mientras el paciente se encuentra en el interior del aparato, se crea un campo magnético que puede generar imágenes. Es muy útil para detectar grasa o pequeñas cicatrices en el corazón, que pueden aparecer en las miocardiopatías. La calidad de las imágenes obtenidas es superior a las de la ecocardiografía.
Cateterismo cardiaco y estudio electrofisiológico
Estas dos pruebas se realizan en la sala de hemodinámica y en el laboratorio de electrofisiología respectivamente. Para realizarlos se utilizan rayos X para visualizar el corazón y el instrumental que se utiliza durante el procedimiento. El médico que realiza la prueba, introduce a través de una arteria (la femoral, en la ingle o la radial en la muñeca) unos catéteres muy finos que llegan hasta el corazón. El paciente debe permanecer acostado en una camilla especial durante el procedimiento, que se realiza con anestesia local.
Durante el cateterismo cardiaco se inyecta un contraste para visualizar las arterias coronarias, para comprobar cómo es la circulación en estas arterias y poder detectar anomalías o estrechamientos en las mismas.
En un estudio electrofisiológico se introducen electrodos dentro del corazón para analizar sus propiedades eléctricas e inducir arritmias. Es de utilidad para diagnosticar y tratar el Síndrome de Wolf-Parkinson-White y decidir el tratamiento del Síndrome de Brugada. El Síndrome de WolfParkinson-White se produce por la existencia de una vía accesoria (unas fibras que no deberían existir que comunica la aurícula con el ventrículo), y durante este estudio, puede localizase con exactitud y quemarla utilizando radiofrecuencia. Este procedimiento se llama ablación y permite curar esta enfermedad.
Test de la mesa basculante o tilt test
Esta prueba se utiliza para estudiar los síncopes, especialmente aquellos conocidos como síncopes neuromediados (también llamados vasovagales o lipotimias), que son especialmente frecuentes en mujeres jóvenes.
Para realizar esta prueba el paciente permanece tumbado en una camilla mientras se controla la tensión arterial, la frecuencia cardiaca y se realiza un ECG. Después la tabla se inclina a 60-75º mientras continúa la monitorización. Si no se reproduce ningún síntoma, se administra nitroglicerina sublingual y se monitoriza al paciente durante 15 minutos más. Pasado este tiempo, la tabla vuelve a una posición horizontal y se da por finalizada la prueba. Si durante la prueba el paciente sufre síntomas, podemos comprobar la tensión arterial y el ritmo cardiaco para poder diagnosticarlo como síncope vasovagal.
¿Qué importancia tiene el análisis genético?
En la mayoría de enfermedades que producen parada cardiaca sin cardiopatía estructural se han detectado mutaciones en ciertos genes que se piensa que pueden producir la enfermedad. Por tanto, si pudiésemos detectar estas mutaciones diagnosticaríamos la enfermedad tanto en el paciente que ha sufrido la parada como en algunos de sus familiares. Desgraciadamente, no siempre es posible realizar este diagnóstico porque no conocemos todos los genes que están involucrados en estas enfermedades. Además, hay que tener en cuenta que existen variaciones en el ADN de muchas personas y esto no significa necesariamente enfermedad. En otras ocasiones se encuentran mutaciones que sólo aparecen en una determinada familia, por lo que resulta difícil decidir si esa mutación es la responsable de la enfermedad. Actualmente se están llevando a cabo investigaciones para conocer mejor los genes que producen estas enfermedades.
¿Qué posibilidades hay de diagnosticar la alteración genética que causa la parada cardiaca?
- En el caso de que el paciente fallezca y no se identifique ninguna alteración en la necropsia, el estudio genético podría llegar al diagnóstico entre el 25-50% de los casos.
- En pacientes diagnosticados de Síndrome de QT largo el diagnóstico genético es positivo en un 50-60% de los pacientes. Los análisis genéticos pueden identificar en ocasiones a los portadores de una mutación responsable de Síndrome de QT largo. Un problema que puede surgir es que una familia puede portar una mutación que no haya sido encontrada en ninguna otra familia. Esto hace que sea difícil saber si esta mutación es la responsable de la enfermedad. Además, si seleccionamos a varias personas con la misma mutación, veremos que unas tienen síntomas y otras no. En definitiva, existe cierta variabilidad en la expresión de la enfermedad entre los portadores de una misma mutación.
- En los pacientes diagnosticados de Síndrome de Brugada el análisis genético sólo será positivo en un 20% de los afectados. Algunas personas que portan el gen mutado pueden tener un test de provocación negativo (no se observan cambios en el ECG al inyectar el antiarrítmico). Estas personas tienen un riesgo muy bajo de sufrir complicaciones.
En los pacientes diagnosticados de taquicardia ventricular catecolaminérgica polimórfica el estudio del gen del receptor de la rianodina es positivo en hasta un 70% de los casos.
A continuación vamos a responder a una serie de preguntas que es posible que se esté planteando acerca de los estudios genéticos:
¿Es posible tener la alteración genética (mutación) y no desarrollar la enfermedad?
La respuesta es sí. Un porcentaje variable de los portadores genéticos pueden no desarrollar la enfermedad. Éste porcentaje es variable según la enfermedad y de forma global ronda un tercio de los portadores. Existen distintas hipótesis para explicar este fenómeno. Es posible que se deba al efecto de factores protectores o que el gen mutado esté en parte inactivado por un fenómeno biológico. En cualquier caso, es importante seguir revisiones periódicas para prevenir complicaciones
¿Tienen el mismo riesgo aquellos afectados de Síndrome de QT largo con un diagnóstico genético que aquellos que no lo tienen?
En general, podemos decir que tienen mayor riesgo los pacientes que tienen un diagnóstico genético. Los pacientes que tienen un QT más largo son los que tienen un mayor riesgo. En estos casos la rentabilidad del estudio genético es mayor. Otra ventaja de tener un diagnóstico genético es que podemos iniciar un tratamiento médico preventivo, que es muy efectivo especialmente en el Síndrome de QT largo tipo I.
¿Por qué es útil tener la información genética si no existe cura para la enfermedad?
El diagnóstico genético permite clasificar adecuadamente a los afectados, diagnosticar precozmente a los portadores genéticos que no han manifestado la enfermedad y diagnosticar casos dudosos. Además, permite tranquilizar a aquellos que no portan la mutación y tiene importantes implicaciones en el consejo genético para la descendencia. Estas enfermedades no son curables pero disponemos de tratamientos médicos eficaces para prevenir las complicaciones.
Recomendaciónes sobre hábitos de vida
Ejercicio físico
La mayoría de las enfermedades que pueden ocasionar una parada cardiaca empeoran con el ejercicio y además, sabemos que el ejercicio físico de competición implica riesgo de complicaciones. Por lo tanto, es recomendable no participar en deportes de competición o en deportes extenuantes. Esto puede ser especialmente difícil en gente joven, por ello hay que hacer un balance entre el beneficio de restringir la actividad física y el impacto negativo que esta restricción puede producir en su desarrollo. Los pacientes diagnosticados de Síndrome de Brugada no requieren limitaciones físicas.
Listado de fármacos a evitar en pacientes con síndrome de QT largo y síndrome de la brugada
Existen ciertos medicamentos que pueden prolongar el intervalo QT. También sabemos que existen medicamentos que deben ser evitados en el Síndrome de Brugada y otros que deben de ser utilizados con precaución. Los más importantes son los antiarrítmicos, ciertos anestésicos, algunos antidepresivos y ciertos antibióticos. La tabla expuesta a continuación muestra los medicamentos de uso más frecuente que pueden prolongar el intervalo QT.
Fármacos a evitar en pacientes con síndrome de QT largo
- Adrenalina
- Dopamina
- Octreotido
- Alfuzosina
- Doxepina
- Ofloxacino
- Amantadita
- Dronedarona
- Ondasetrón
- Amiodarona
- Droperidol
- Paroxetina
- Amitriptilina
- Efedrina
- Pentamidina
- Anfetamina
- Eritromicina
- Procainamida
- Astemizol
- Escitalopram
- Quetiapina
- Atazanavir
- Fenitoína
- Quinidina
- Atomoxetina
- Flecainida
- Ranolazina
- Acitromicina
- Fluconazol
- Risperidona
- Beperidilo
- Fluoxetina
- Ritodrine
- Cloroquina
- Foscarnet
- Ritonavir
- Clorpromacina
- Galantamina
- Salbutamol
- Ciprofloxacino
- Haloperidol
- Salmeterol
- Cisaprida
- Ibutilida
- Sertralina
- Citalopram
- Imipramina
- Sibutramina
- Claritromicina
- Indapamida
- Sotalol
- Clomipramina
- Isoproterenol
- Tacrólimus
- Clozapina
- Itraconazol
- Tamoxifeno
- Cocaína
- Ketoconazol
- Terbutalina
- Desipramina
- Lapatinib
- Terfenadina
- Dexmetilfenidato
- Levofloxacino
- Tioridazina
- Difenidramina
- Litio
- Trazodona
- Disopiramida
- Metadona
- Trimetroprim-sulfametoxazol
- Dobutamina
- Metilfenidato
- Vardenafilo
- Dofetilida
- Moxifloxacino
- Venlafaxina
- Dolasetron
- Nicardipino
- Voriconazol
- Domperidona
- Noradrenalina
- Ziprasidona
Fármacos a evitar siempre en el síndrome de brugada
- Antidepresivos: Amitriptilina; Clomipramina; Litio; Loxapina; Nortriptilina.
- Antiarrítmicos: Ajmalina; Flecainida; Procainamida; Propafenona.
- Anestésicos: Bupivacaína; Propofol.
Fármacos a evitar en la medida de lo posible en síndrome de brugada
- Antiarrítmicos: Amiodarona; Disopiramida; Lidocaína; Propranolol; Verapamil.
- Antidepresivos y antiepilépticos: Carbamazepina; Fluoxetina; Fluvoxamina; Imipramina; Fenitoína; Tioridacina.
- Analgésicos y anestésicos: Ketamina; Tramadol.
Glosario de términos médicos de interés
ADN: Es el código genético. Cada persona recibe una copia de su padre o otra de su madre.
Aorta: Arteria que se origina en el ventrículo izquierdo del corazón y transporta la sangre al resto del organismo.
Arritmia: Alteración del ritmo cardiaco. Ciertas arrítmias, como las ventriculares, pueden ser potencialmente mortales.
Asistolia: Parada cardiaca producida por el cese de la actividad eléctrica del corazón.
Aurícula: Las aurículas son dos cámaras cardiacas cuya función es recibir la sangre de las venas y enviarlas a los ventrículos.
Autopsia: Estudio realizado a un cadáver para establecer las causas de la muerte.
Bloqueo auriculoventricular: Dificultad o imposibilidad del impulso eléctrico caradiaco para pasar de las aurícular a los ventrículos.
Bradicardia: Ritmo cardiaco lento, por debajo de 60 latidos por minuto.
Canal iónico: Es una especie de túnel que se encuentra en la memebrana de las células. Cada canal permite el paso de un ion determinado (Ej: sodio, potasio, calcio¿).
Canalopatía: Enfermedad que afecta a los canales iónicos. Son ejemplos el Síndrome de QT largo hereditario y el Síndrome de Brugada.
DAI: Desfibrilador automático implantable. Es un pequeño aparato que se implanta debajo de la piel. Controla el ritmo cardiaco y si detecta una arritmia potencialmente peligrosa envía una serie de impulsos para restaurar el ritmo cardiaco normal. Si no lo consigue tras un tiempo predeterminado, envía una descarga eléctrica. Cuando el paciente sufre una descarga de DAI debe acudir al hospital.
Desfibrilador: Aparato que es capaz de enviar una descarga eléctrica al corazón y restaurar el ritmo normal.
Enfermedad congénita cardiaca: Enfermedad cardiaca presente desde el nacimiento.
Fármacos antiarritmicos: Medicamentos que pueden ser utilizados para regular y mantener el ritmo cardiaco normal. Algunos de estos fármacos pueden ser utilizados para diagnosticar el síndrome de Brugada, como la flecainida o la ajmalina.
Gen: Fragmento de ADN responsable de la producción de una proteína.
Ion: sustancia química que contiene una carga eléctrica. Son fundamentales para el funcionamiento eléctrico del corazón. Fundamentalmente sodio, potasio y calcio.
Marcapasos: Dispositivo que se implanta debajo de la piel, cerca del hombro izquierdo. De él surgen 1, 2 o 3 cables que van al corazón. Este aparato controla el ritmo del corazón y, cuando este falla, envía impulsos eléctricos para que el corazón se contraiga.
Miocardiopatía: Enfermedad del músculo cardiaco. Es muchas ocsiones es hereditaria.
Mutación: Anomalía en un gen que produce una anomalía en una proteína o en su función. Puede heredarse de los padres. En ocasiones, el enfermo es el primero en padecer la mutación (mutación esporádica).
Parada cardiaca: Situación en la que el corazón no bombea sangre suficiente para oxigenar a los órganos.
QT: es un intervalo medible del ECG. Se encuentra prolongado en el Síndrome de QT largo, aunque puede alargarse por otras causas.
